,
содержат связь NaЧС. Соед. AlkNa-бесцв. неплавкие в-ва, не раств. в углеводородах; ArNa и жирно-ароматич. Н. с.-твердые интенсивно окрашенные в-ва, не раств. в углеводородах, раств. в простых эфирах (иногда с разрывом связи СЧО); анион-радикальные Н. с. типа Na+[ArH]_Х плохо раств. в диэтиловом эфире; CH=CNa-слабо окрашенное твердое в-во; C5H5Na-6ecцв. кристаллы, не раств. в большинстве орг. р-рителей, раств. в ТГФ и жидком NH3.
Структура Н. с. установлена лишь для нек-рых соед., напр. CH3Na, по-видимому, тетрамср аналогично CH3Li; комплекс C5H5NaХL [L = (СН 3)2 NCH2CH2N (CH3)2] представляет собой цепочку из С 5 Н 5 -колец, связанных мостиковыми фрагментами NaХL. В р-рах Н. с. связи СЧN
…
Далее
,
содержат связь NaЧС. Соед. AlkNa-бесцв. неплавкие в-ва, не раств. в углеводородах; ArNa и жирно-ароматич. Н. с.-твердые интенсивно окрашенные в-ва, не раств. в углеводородах, раств. в простых эфирах (иногда с разрывом связи СЧО); анион-радикальные Н. с. типа Na+[ArH]_Х плохо раств. в диэтиловом эфире; CH=CNa-слабо окрашенное твердое в-во; C5H5Na-6ecцв. кристаллы, не раств. в большинстве орг. р-рителей, раств. в ТГФ и жидком NH3.
Структура Н. с. установлена лишь для нек-рых соед., напр. CH3Na, по-видимому, тетрамср аналогично CH3Li; комплекс C5H5NaХL [L = (СН 3)2 NCH2CH2N (CH3)2] представляет собой цепочку из С 5 Н 5 -колец, связанных мостиковыми фрагментами NaХL. В р-рах Н. с. связи СЧNa обладают значительно большим ионным характером, чем связи СЧLi в литийорганических соединениях. В зависимости от типа Н. с. и природы среды в р-ре могут присутствовать отдельные ионы R- и Na+ , сольватно-разделенные и контактные ионные пары, либо существует равновесие между этими формами.
Н. с. очень чувствительны к О 2 воздуха и следам влаги (работают с ними в инертной атмосфере); на воздухе самовоспламеняются, C5H5Na обугливается, ArNa при осторожном окислении флуоресцируют. При нагр. без доступа воздуха AlkNa разлагаются с образованием NaH и олефинов; ArNa, HC=CNa и C5H5Na устойчивы к нагреванию. Н. с. карбеноидного типа RR'C(Na)Hal или o-NaC6H4Hal при термич. разложений образуют карбены RR'C: или дегидро-бензол.
Вода, к-ты, спирты разлагают Н. с. (иногда с возгоранием или взрывом). Н. с. взаимод. с СО 2, давая соли карбоновых к-т, и алкилирующими агентами; эти р-ции прогекают с сохранением конфигурации у sp3 -гибридизованного атома С, тогда как р-ции с галогенами протекают с обращением конфигурации. С карбонильными соед. Н. с. реагируют подобно литийорг. и магнийорг. соед. (см. Гриньяра реакция), однако в отличие от них AlkNa и ArNa разрывают связь СЧО в простых эфирах, напр. С 2 Н 5 ОС 2 Н 5 + + C2H5Na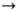 C2H5ONa + С 2 Н 4 + С 2 Н 6. Н. с. присоединяются по кратным связям, вступают в р-цию переметаллиро-вания, металлируют углеводороды с подвижным атомом водорода, взаимод. с галогенидами металлов с образованием металлоорг. соединений. Анион-радикальные Н. с. типа Na+ [АrН]_Х присоединяют атом Н с образованием продуктов восстановления, напр. при гидролизе C10Hg8_Х Na+ образуется 1,4-дигидронафталин. Для Н. с. характерны карб-анионные сигматропные согласованные перегруппировки, напр.
C2H5ONa + С 2 Н 4 + С 2 Н 6. Н. с. присоединяются по кратным связям, вступают в р-цию переметаллиро-вания, металлируют углеводороды с подвижным атомом водорода, взаимод. с галогенидами металлов с образованием металлоорг. соединений. Анион-радикальные Н. с. типа Na+ [АrН]_Х присоединяют атом Н с образованием продуктов восстановления, напр. при гидролизе C10Hg8_Х Na+ образуется 1,4-дигидронафталин. Для Н. с. характерны карб-анионные сигматропные согласованные перегруппировки, напр. 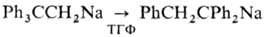 . Н. с. образуют комп лексы с др. металлоорг. соед., напр. Na+ [Ph2Li]-, к-рые устойчивы к простым эфирам (в отличие от PhNa).
. Н. с. образуют комп лексы с др. металлоорг. соед., напр. Na+ [Ph2Li]-, к-рые устойчивы к простым эфирам (в отличие от PhNa).
Н. с. обычно используют в виде суспензий или р-ров в орг. р-рителях, при упаривании к-рых м. б. получены индивидуальные твердые соединения. Осн. способы получения Н. с.: 1) взаимод. RCl с тонкодисперсным Na или амальгамой Na в орг. р-рителях; способ
…
Перейти к полному виду статьи
Свернуть
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.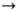 C2H5ONa + С 2 Н 4 + С 2 Н 6. Н. с. присоединяются по кратным связям, вступают в р-цию переметаллиро-вания, металлируют углеводороды с подвижным атомом водорода, взаимод. с галогенидами металлов с образованием металлоорг. соединений. Анион-радикальные Н. с. типа Na+ [АrН]_Х присоединяют атом Н с образованием продуктов восстановления, напр. при гидролизе C10Hg8_Х Na+ образуется 1,4-дигидронафталин. Для Н. с. характерны карб-анионные сигматропные согласованные перегруппировки, напр.
C2H5ONa + С 2 Н 4 + С 2 Н 6. Н. с. присоединяются по кратным связям, вступают в р-цию переметаллиро-вания, металлируют углеводороды с подвижным атомом водорода, взаимод. с галогенидами металлов с образованием металлоорг. соединений. Анион-радикальные Н. с. типа Na+ [АrН]_Х присоединяют атом Н с образованием продуктов восстановления, напр. при гидролизе C10Hg8_Х Na+ образуется 1,4-дигидронафталин. Для Н. с. характерны карб-анионные сигматропные согласованные перегруппировки, напр. 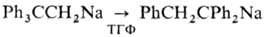 . Н. с. образуют комп лексы с др. металлоорг. соед., напр. Na+ [Ph2Li]-, к-рые устойчивы к простым эфирам (в отличие от PhNa).
. Н. с. образуют комп лексы с др. металлоорг. соед., напр. Na+ [Ph2Li]-, к-рые устойчивы к простым эфирам (в отличие от PhNa).