происходят с обменом атомов или групп атомов в молекуле на др. атомы или группы; обозначаются символом S (от лат. substitutio - замещение). В зависимости от способа расщепления связи элемент - уходящая группа (с распариванием пары электронов или ее сохранением) различают р-ции гомолитич. (
<>R)
и гетеролитич. замещения; последние в зависимости от того, у какого атома остается пара электронов, подразделяют на р-ции нуклеоф. (
<>N)
или электроф. (
<> Е) замещения, напр.:
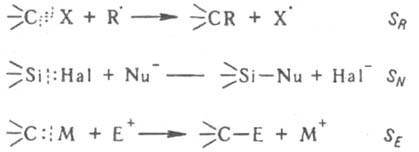
В р-циях гетеролитич. замещения нуклеоф. частица часто предоставляет свою электронную пару для образования новой связи не сразу, а постадийно, т. е. реализуется механизм замещения с переносом электрона и образованием промежут. анион-радикальных частиц (напр., по механизму
<>RN1):
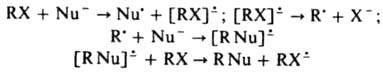
Иногда бывает трудно отнести замещение к к.-л. определенному типу, поскольку классификация зависит от того, какую молекулу считают субстратом, а какую - реагентом. Напр., р-ция Вюрца RЧHal + R'M : RЧR' + MHal - S
N -р-ция по отношению к RNal и S
E - пo отношению к R'ЧМ. Гомолитич. путь замещения у насыщ. атома углерода осуществляется в осн. по цепному радикальному механизму и характеризуется стадиями инициирования, роста и обрыва цепи (см.
Радикальные реакции). К важнейшим р-циям этого типа относятся гомолитич. хлорирование (металепсия), радикальное нитрование (р-ция Коновалова), окисление углеводородов. Электроф. и нуклеоф. 3. р. в зависимости от кинетич. закономерностей разделяются на би- и мономолекулярные. Бимолекулярное замещение (
<>N2
и
<>E2) осуществляется через переходное состояние, в к-ром происходит одновременное образование новой и разрыв старой связи. При мономолекулярном замещении атакующий агент (нуклеофил или электрофил) не принимает участия в лимитирующей стадии р-ции, а в молекуле субстрата происходит разрыв связи с образованием карбкатиона (механизм
<>N1), карбаниона (механизм
<> Е1) или соответствующих им ионных пар
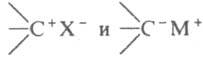
Стереохим. результат замещения зависит от конкретного механизма р-ции и природы реагирующих соединений. Р-ции
<>N2 в осн. протекают с обращением конфигурации оптически активного атома углерода, р-ции S
Е 2 соединений с s-связью углерод - металл в осн. с сохранением конфигурации. Остальные варианты замещения у алифатич. атома углерода не стереоспецифичны. Нуклеоф. замещение у ненасыщ. атома углерода обычно характеризуется первонач. присоединением агента по кратной связи с образованием интермедиата и послед. отщеплением уходящей группы, напр., при арилировании алкенов по Хеку, ацилировании аминов, димеризации ацетиленидов по Кадио-Ходкевичу:
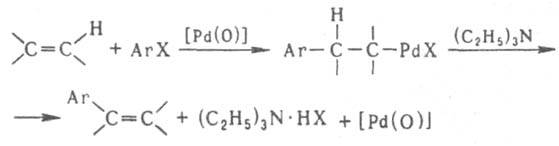
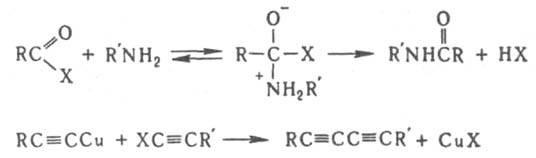
В ароматич. ряду механизмы 3. р. более разнообразны. Наиб. изучено электроф. ароматич. замещение (
<>E Аr), протекающее с промежут. образованием катионного s-комплекса (см.
Ароматические соединения). К этому типу замещения относятся р-ции нитрования, сульфирования, азосочетания, алкилирования и ацилирования по Фриделю Крафтсу и др., причем скорость р-ции и место вхождения заместителя зависят от природы присутствующих в субстрате групп (ориентанты первого и второго рода). В качестве уходящей группы выступает обычно водород, хотя известны примеры замещения одной группы на другую (
unсо -замещение). Нуклеоф. замещение в электронодефицитной ароматич. молекуле протекает чаще всего через стадию образования анионного s-комплекса. Др. важнейшие механизмы нуклеоф. замещения в ароматич. ряду механизм
<>RN1 и ариновый, характеризующийся возникновением дегидробензолов. Изменение условий протекания одной и той же р-ции может привести к изменению механизма процесса и строения продуктов, напр.:
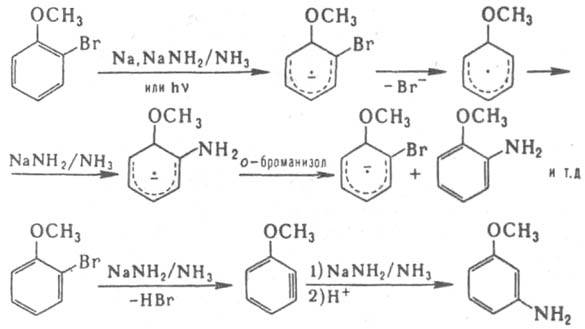
В гетероциклич. ряду 3. р. могут происходить с участием как заместителей, так и атомов самого кольца. Примеры последнего варианта замещения р-ция Юрьева для взаимных превращ. пиррола, фурана и тиофена, а также р-ции, протекающие по механизму ANRORC. Эти р-ции протекают с раскрытием цикла и послед. его замыканием, напр.:
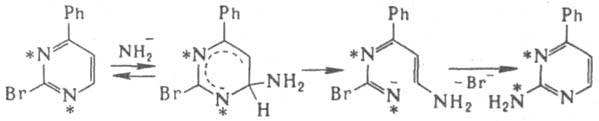
В химии неорг. соед. примерами 3. р. являются обмен лигандов в
координационных соединениях, вытеснение металла из соли под действием др. металла и т. д., напр.:
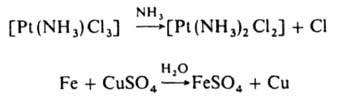
Независимо от механизма р-ции, к-рый в последнем случае относится к окислит-восстановит. типу, результат процесса - замещение. См. также
Нуклеофильные реакции, Одноэлектронный перенос. Электрофильные реакции. Лит.: Басоло Ф., Пирсон Р. Механизмы неорганических реакций, пер. с англ., М. 1971. Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов. Л., 1980. с. 62-90 Общая органическая химия, пер. с aнгл. т. 1. ч. 2. М., 1981; там же. т. 7. ч. 15. М., 1984; Росси Р. А., Росси Р. X. де. Ароматическое замещение по механизму
<>RH,
пер. с англ., М., 1986.
Д. В. Давыдов.
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.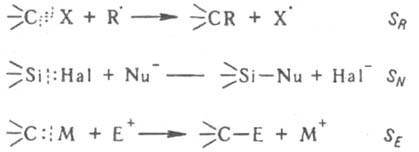 В р-циях гетеролитич. замещения нуклеоф. частица часто предоставляет свою электронную пару для образования новой связи не сразу, а постадийно, т. е. реализуется механизм замещения с переносом электрона и образованием промежут. анион-радикальных частиц (напр., по механизму <>RN1):
В р-циях гетеролитич. замещения нуклеоф. частица часто предоставляет свою электронную пару для образования новой связи не сразу, а постадийно, т. е. реализуется механизм замещения с переносом электрона и образованием промежут. анион-радикальных частиц (напр., по механизму <>RN1): 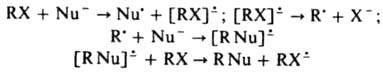 Иногда бывает трудно отнести замещение к к.-л. определенному типу, поскольку классификация зависит от того, какую молекулу считают субстратом, а какую - реагентом. Напр., р-ция Вюрца RЧHal + R'M : RЧR' + MHal - SN -р-ция по отношению к RNal и SE - пo отношению к R'ЧМ. Гомолитич. путь замещения у насыщ. атома углерода осуществляется в осн. по цепному радикальному механизму и характеризуется стадиями инициирования, роста и обрыва цепи (см. Радикальные реакции). К важнейшим р-циям этого типа относятся гомолитич. хлорирование (металепсия), радикальное нитрование (р-ция Коновалова), окисление углеводородов. Электроф. и нуклеоф. 3. р. в зависимости от кинетич. закономерностей разделяются на би- и мономолекулярные. Бимолекулярное замещение (<>N2 и <>E2) осуществляется через переходное состояние, в к-ром происходит одновременное образование новой и разрыв старой связи. При мономолекулярном замещении атакующий агент (нуклеофил или электрофил) не принимает участия в лимитирующей стадии р-ции, а в молекуле субстрата происходит разрыв связи с образованием карбкатиона (механизм <>N1), карбаниона (механизм <> Е1) или соответствующих им ионных пар
Иногда бывает трудно отнести замещение к к.-л. определенному типу, поскольку классификация зависит от того, какую молекулу считают субстратом, а какую - реагентом. Напр., р-ция Вюрца RЧHal + R'M : RЧR' + MHal - SN -р-ция по отношению к RNal и SE - пo отношению к R'ЧМ. Гомолитич. путь замещения у насыщ. атома углерода осуществляется в осн. по цепному радикальному механизму и характеризуется стадиями инициирования, роста и обрыва цепи (см. Радикальные реакции). К важнейшим р-циям этого типа относятся гомолитич. хлорирование (металепсия), радикальное нитрование (р-ция Коновалова), окисление углеводородов. Электроф. и нуклеоф. 3. р. в зависимости от кинетич. закономерностей разделяются на би- и мономолекулярные. Бимолекулярное замещение (<>N2 и <>E2) осуществляется через переходное состояние, в к-ром происходит одновременное образование новой и разрыв старой связи. При мономолекулярном замещении атакующий агент (нуклеофил или электрофил) не принимает участия в лимитирующей стадии р-ции, а в молекуле субстрата происходит разрыв связи с образованием карбкатиона (механизм <>N1), карбаниона (механизм <> Е1) или соответствующих им ионных пар 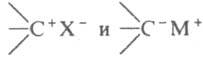 Стереохим. результат замещения зависит от конкретного механизма р-ции и природы реагирующих соединений. Р-ции <>N2 в осн. протекают с обращением конфигурации оптически активного атома углерода, р-ции S Е 2 соединений с s-связью углерод - металл в осн. с сохранением конфигурации. Остальные варианты замещения у алифатич. атома углерода не стереоспецифичны. Нуклеоф. замещение у ненасыщ. атома углерода обычно характеризуется первонач. присоединением агента по кратной связи с образованием интермедиата и послед. отщеплением уходящей группы, напр., при арилировании алкенов по Хеку, ацилировании аминов, димеризации ацетиленидов по Кадио-Ходкевичу:
Стереохим. результат замещения зависит от конкретного механизма р-ции и природы реагирующих соединений. Р-ции <>N2 в осн. протекают с обращением конфигурации оптически активного атома углерода, р-ции S Е 2 соединений с s-связью углерод - металл в осн. с сохранением конфигурации. Остальные варианты замещения у алифатич. атома углерода не стереоспецифичны. Нуклеоф. замещение у ненасыщ. атома углерода обычно характеризуется первонач. присоединением агента по кратной связи с образованием интермедиата и послед. отщеплением уходящей группы, напр., при арилировании алкенов по Хеку, ацилировании аминов, димеризации ацетиленидов по Кадио-Ходкевичу: 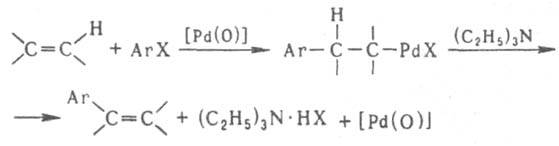
 В ароматич. ряду механизмы 3. р. более разнообразны. Наиб. изучено электроф. ароматич. замещение (<>E Аr), протекающее с промежут. образованием катионного s-комплекса (см. Ароматические соединения). К этому типу замещения относятся р-ции нитрования, сульфирования, азосочетания, алкилирования и ацилирования по Фриделю Крафтсу и др., причем скорость р-ции и место вхождения заместителя зависят от природы присутствующих в субстрате групп (ориентанты первого и второго рода). В качестве уходящей группы выступает обычно водород, хотя известны примеры замещения одной группы на другую (unсо -замещение). Нуклеоф. замещение в электронодефицитной ароматич. молекуле протекает чаще всего через стадию образования анионного s-комплекса. Др. важнейшие механизмы нуклеоф. замещения в ароматич. ряду механизм <>RN1 и ариновый, характеризующийся возникновением дегидробензолов. Изменение условий протекания одной и той же р-ции может привести к изменению механизма процесса и строения продуктов, напр.:
В ароматич. ряду механизмы 3. р. более разнообразны. Наиб. изучено электроф. ароматич. замещение (<>E Аr), протекающее с промежут. образованием катионного s-комплекса (см. Ароматические соединения). К этому типу замещения относятся р-ции нитрования, сульфирования, азосочетания, алкилирования и ацилирования по Фриделю Крафтсу и др., причем скорость р-ции и место вхождения заместителя зависят от природы присутствующих в субстрате групп (ориентанты первого и второго рода). В качестве уходящей группы выступает обычно водород, хотя известны примеры замещения одной группы на другую (unсо -замещение). Нуклеоф. замещение в электронодефицитной ароматич. молекуле протекает чаще всего через стадию образования анионного s-комплекса. Др. важнейшие механизмы нуклеоф. замещения в ароматич. ряду механизм <>RN1 и ариновый, характеризующийся возникновением дегидробензолов. Изменение условий протекания одной и той же р-ции может привести к изменению механизма процесса и строения продуктов, напр.:  В гетероциклич. ряду 3. р. могут происходить с участием как заместителей, так и атомов самого кольца. Примеры последнего варианта замещения р-ция Юрьева для взаимных превращ. пиррола, фурана и тиофена, а также р-ции, протекающие по механизму ANRORC. Эти р-ции протекают с раскрытием цикла и послед. его замыканием, напр.:
В гетероциклич. ряду 3. р. могут происходить с участием как заместителей, так и атомов самого кольца. Примеры последнего варианта замещения р-ция Юрьева для взаимных превращ. пиррола, фурана и тиофена, а также р-ции, протекающие по механизму ANRORC. Эти р-ции протекают с раскрытием цикла и послед. его замыканием, напр.:  В химии неорг. соед. примерами 3. р. являются обмен лигандов в координационных соединениях, вытеснение металла из соли под действием др. металла и т. д., напр.:
В химии неорг. соед. примерами 3. р. являются обмен лигандов в координационных соединениях, вытеснение металла из соли под действием др. металла и т. д., напр.: 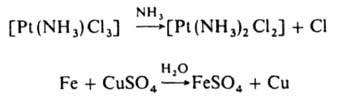 Независимо от механизма р-ции, к-рый в последнем случае относится к окислит-восстановит. типу, результат процесса - замещение. См. также Нуклеофильные реакции, Одноэлектронный перенос. Электрофильные реакции. Лит.: Басоло Ф., Пирсон Р. Механизмы неорганических реакций, пер. с англ., М. 1971. Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов. Л., 1980. с. 62-90 Общая органическая химия, пер. с aнгл. т. 1. ч. 2. М., 1981; там же. т. 7. ч. 15. М., 1984; Росси Р. А., Росси Р. X. де. Ароматическое замещение по механизму <>RH, пер. с англ., М., 1986. Д. В. Давыдов.
Независимо от механизма р-ции, к-рый в последнем случае относится к окислит-восстановит. типу, результат процесса - замещение. См. также Нуклеофильные реакции, Одноэлектронный перенос. Электрофильные реакции. Лит.: Басоло Ф., Пирсон Р. Механизмы неорганических реакций, пер. с англ., М. 1971. Эфрос Л. С., Горелик М. В., Химия и технология промежуточных продуктов. Л., 1980. с. 62-90 Общая органическая химия, пер. с aнгл. т. 1. ч. 2. М., 1981; там же. т. 7. ч. 15. М., 1984; Росси Р. А., Росси Р. X. де. Ароматическое замещение по механизму <>RH, пер. с англ., М., 1986. Д. В. Давыдов.