(кислотно-основный катализ), ускорение хим. р-ций в присут. к-т и оснований. В качестве катализаторов используют: в гомог. кислотном катализе протонные к-ты (H
2SO
4, HCl, Н
3 РО
4, CH
3C
6H
4SO
2OH и др.) в воде и водно-орг. р-рителях, апротонные к-ты (АlС1
3, BF
3, SnCl
4 и др.) в неводных р-рителях, сверхкислоты (HF SbF
5, HSO
3F SbF
5 и др.) в неводных р-рителях; в гетерог. кислотном катализе прир. глины, аморфные и кристаллич. алюмосиликаты, фосфорную и полифосфорные к-ты, нанесенные на носитель, катиониты; в гомог. основном катализе оксиды щелочных металлов, амины в воде, орг. и водно-орг. р-рителях; в гетерог основном катализе - оксиды металлов (CaO, MgO и др.). При К.-о. к. в большинстве случаев из реагентов и катализатора в равновесных стадиях образуются реакционноспособные (а также нереакционноспособные) комплексы разл. состава, к-рые являются ионизир. формой реагента. В лимитирующих стадиях комплексы превращ. в продукты р-ции. В случае р-ции с одним реагентом (Р) эти стадии выражаются ур-нием:
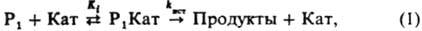
где Кат-разл. формы катализатора: недиссоциир. к-ты или основания, ионы или ионные пары, образующиеся при их ионизации; P
1 Кат-комплексы; К
i - константа равновесия образования комплексов Р
1 Кат; k
ист - элементарная константа скорости превращ. комплексов в продукты. В случае р-ции двух реагентов (P
1+Р
2: Продукты; Р
2+Р
2: Продукты) реакционноспособный комплекс образуется, как правило, из комплекса одного реагента с несвязанным в комплекс др. реагентом:
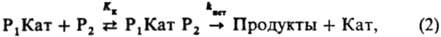
где К
к -константа равновесия образования комплексов Р
1 Kат Р
2. Константы равновесия K
i и К
к выражают ур-ниями:
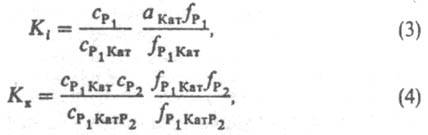
где (здесь и далее)
а, с, f -соотв. термодинамич. активность, концентрация и коэф. активности реагирующих частиц; a
Kатf
P1/f
P1Кат - ф-ция, характеризующая способность среды переводить реагенты в комплексы РКат. При варьировании в широких пределах с
Кат реализуются (особенно в р-рах) неск. маршрутов р-ции - хим. превращений, приводящих к образованию одних и тех же продуктов через реакционноспособные комплексы (РК) разл. состава. В р-ре с постоянной с
Кат скорость р-ции по каждому маршруту W
i выражается ур-нием:
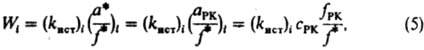
где (k
ист)
i - элементарная константа скорости по i-му маршруту, а* и f* - относятся к активир. комплексу. Из опытных данных следует, что множитель f
РК/f* не изменяется при варьировании с
Кат и его приравнивают к единице. В р-ре с постоянной с
Кат наблюдаемая скорость р-ции
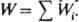
Экспериментально определяют эффективную константу скорости k
эфф, характеризующую скорость р-ции при постоянной т-ре и наличии катализатора определенного состава. В ур-ниях для связи f
эфф со св-вами катализатора учитывают все его комплексы с реагентом: реакционноспособные (РКат)
РК и нереакционноспособные (РКат)
НРК. Напр., при кислотном гидролизе амидов, анилидов ионизированная по атому азота форма является реакционноспособной, ионизированная по карбонильной группе - либо намного менее реакционноспособна, либо нереакционноспособна. Для описания влияния ионизирующих св-в среды на k
эфф совместно решают ур-ние материального баланса для текущих концентраций реагентов и ур-ния (3) и (5) в случае р-ции одного реагента и дополнительно ур-ние (4) для р-ции двух реагентов. напр. для р-ции, протекающей по схеме (2):

В случае р-ции двух реагентов, если один (Р
2) является компонентом р-рителя (напр., Н
2 О при гидролизе в водных р-рах), при условии с
р2>>е
р1 вычисляют эффективную константу скорости первого порядка, включающую термодинамич. активность р-рителя. В р-циях Р
х с Р
2 в р-рах к-т и оснований реакционноспособный комплекс состава P
1KaтP
2 может получаться и в лимитирующей стадии из ионизир. формы одного реагента и неионизир. формы другого:
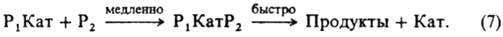
В этом случае для описания влияния ионизирующих св-в среды на k
эфф пригодно ур-ние (6), при замене величины (f
P2 с
P2)/(К
кf
P1КатP2) на термодинамич. активность растворителя. Поскольку крайне редко удается установить прямыми физ. методами состав и концентрацию промежут. комплексов, в настоящее время основным методом установления их состава, детального механизма р-ции и вычисления величин К
i и К
к является кинетич. метод, основанный на применении ур-ний типа (6) для объяснения наблюдаемой зависимости k
эфф от ионизирующей способности среды. Для этого измеряют k
эфф в широком диапазоне с
Кат в р-ре и подбирают ф-ции а
Кат f
P/f
PКат для описания влияния среды на k
эфф. наиб. исследованы каталитич. св-ва сильных к-т в водных р-рах. Ионизирующая способность таких р-ров обусловлена образованием комплексов реагента: 1) с сольватированным протоном и 2) с недиссоциированной к-той. К первым относятся протонир. форма реагента и ее комплексы с р-рителем. В этом случае а
Катf
P/f
PKат выражают (для водных р-ров) ф-циями h
0 =a
H3O+f
P/f
PH+, h
0a
H2O и h
0a
2 Н2O, где h
0 - измеренная индикаторным методом кислотность среды, f
РН+ -коэф. активности протонир. формы реагента. Ко вторым относятся комплексы реагента с к-той (НА) и ее гидратами. При этом a
Катf
Р/f
РКат кат принимает значения а
НА, a
НАa
Н2O и др. При гидролизе нек-рых карбонильных соед. a
Катf
P/f
РКат=c
H5O2+ Однозначную информацию о составе реакционноспособных комплексов, как правило, получают на основании данных по изменению k
эфф в р-рителе постоянного состава при варьировании с
Кат в широких пределах в условиях малой степени связывания реагента в комплексы. наиб. простые зависимости получают для р-ции одного реагента, когда он равновесно связывается только в один реакционноспособный комплекс. В таком случае ур-ние (4) упрощается:
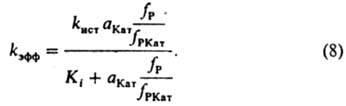
Опытным путем установлено, что в водных р-рах сильных к-т k
ист не зависит от с
Кат. К
i, по определению, не должно зависеть от с
Кат. Вопрос о влиянии состава смешанного р-рителя на k
ист пока достаточно не исследован. В условиях, когда K
i и (a
Катf
Р)/f
РКат соизмеримы, по ур-нию (8) вычисляют раздельно k
ист и K
i.
При а
Катf
Р/f
РКат >> K
i<> величина k
эфф=k
ист; при k
Катf
P/f
РКат<<K
i имеет место соотношение:
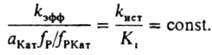
Ниже приведен пример, раскрывающий природу каталитич. действия водных р-ров к-т в условиях, когда реакционноспособный комплекс образуется и превращ. в продукты согласно схеме (1) при условии, что а
Катf
P/f
РКат<<K
i. Ионизирующая способность среды из-за превращ. реагента в протонир. форму и ее комплексы с Н
2 О проявляется при наличии зависимостей К
эфф/h
0=const, k
эфф(h
0a
H2О)=const k
эфф/(h
0a
2H2O)=const. Если в р-ции k
эфф/h
0=const (lgk
эфф+H
0=const, где H
0=-lgh
0 - ф-ция кислотности Гаммета), то a
катf
P/f
Кат=h
0 и реакционноспособным комплексом является протонир. форма реагента РН
3 О
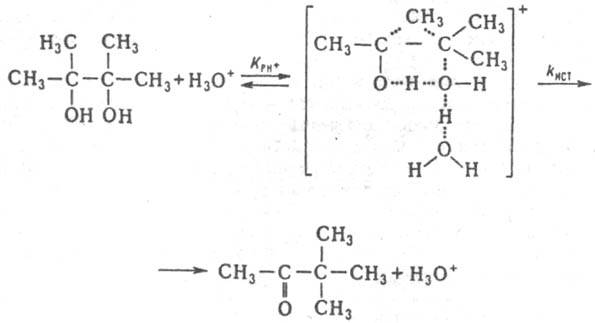
+. Такая закономерность имеет место при проведении пинаколиновой перегруппировки в конц. H
2SO
4:
При варьировании с
Kaт значение k
эфф/(h
0 а
H2O) постоянно в р-циях дегидратации, напр. 2-фенил-2-пропанола в серной к-те, 2-метил-2-бутанола в азотной к-те. Следовательно, а
Kатf
P/f
PKaт равно h
0 а
H2O и реакционноспособным является комплекс молекулы воды с протонир. формой реагента. Имеется и пример постоянства k
эфф/(h
0a
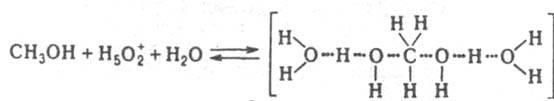
2H2O), что наблюдается в р-ции изотопного обмена атома кислорода в СН
3 ОН, протекающего в серной и хлорной к-тах. В этом случае а
Kaт/f
P/f
РКaт=h
0a
2H2O и реакционноспособным является симметричный комплекс:
Ф-ции h
0, h
0 а
H2O и h
0 а
2H2O стандартизованы к воде, и в сильно разбавленных р-рах сильных к-т они численно равны концентрации ионов Н
5 О
+2 в моль/л. В таких р-рах для приведенных выше р-ций при варьировании с
Kaт должно соблюдаться постоянство значений k
эфф/c
H2O+. При гидролизе нек-рых амидов, анилидов, сложных эфиров k
эфф/c
H2O+ постоянно не только в разбавленных, но и в конц. водный р-рах НСlO
4, H
2SO
4. Если гидролиз протекает по схеме (1), то реакционноспособный комплекс образуется из реагента и иона Н
5 О
2+, а выраженная в концентрациях константа равновесия K
H5O2+; не изменяется при варьировании с
Кат:
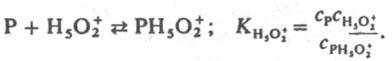
Не исключено, что k
эфф/c
H2O+=const из-за того, что р-ция протекает по схеме (7) Ионизирующая способность среды из-за комплексообразования реагента с молекулами недиссоциир. сильной к-ты и ее гидратом проявляется при наличии зависимостей k
эфф/a
HA=const, k
эфф/(a
HAa
H2O)=const и др. В первом случае a
Kaт=const и реакци онноспособный комплекс имеет состав РИА; такая закономерность, напр., реализуется при дегидратации b-фенил-b-гидроксипропионовой к-ты и 2-(4-мето-ксифенил)-2-пропанола в серной к-те. Во втором случае а
катf
P/f
PKат=а
HА а
H2O и комплекс имеет состав РНАН
2 О. Гидрат НА. Н
2 О можно рассматривать и как ионную пару Н
3 О
+ А
-. Каталитич. активность гидратов сильных к-т проявляется в р-циях дегидратации 1-фенилэтанола в хлорной к-те, гидратации
цис -коричной к-ты и рацемизации b-фенил-b-гидроксипропионовой к-ты в серной к-те. Согласно ур-нию (6), должен наблюдаться максимум k
эфф в зависимости от с
Кат, если наряду с реакционноспособными образуются и нереакционноспособные комплексы и при увеличении с
Кат значение a
Кат/f
P/f
PKат для нeрeакционноспособных комплексов возрастает быстрее и более резко, чем для реакционноспособных. Напр., если a
Катf
P/f
PKaт равно с
H5O2+ для реакционноспособных комплексов и равно h
0, либо h
0a
H2O для нереакционноспособных. В водных р-рах слабых к-т каталитич. активность проявляют ионы и недиссоциир. молекулы к-ты. Взаимосвязь между каталитич. активностью слабых к-т и их константами диссоциации в нек-рых случаях удается описать корреляц. ур-нием Брёнстеда. В сильно разбавленных водных р-рах оснований ндблюдается постоянство k
эфф/c
OH -при варьировании с
OH-. Обоснованных количеств. характеристик ионизирующей способности умеренно конц. и конц. р-ров оснований пока нет. Добавление солей к водным р-рам к-т и оснований существенно изменяет их каталитич. активность; в случае слабых к-т и оснований изменяется степень их диссоциации на ионы из-за наличия общего иона и увеличения ионной силы р-ра. В случае сильных к-т изменяются величины h
0, а
НА, а
Н2O, что приводит к увеличению относит, концентрации комплексов, образующихся из частиц Н
3 О
+ А
-, НА, а также усилению реакц. способности ионов Н
5 О
2+, напр. при гидролизе в условиях, когда a
Катf
P/f
PKат=с
H2O+. В случае сильных оснований катионы металлов усиливают каталитич. действие сольватир. ионов ОН
-. Лимитирующие стадии катализируемых к-тами и основаниями р-ций часто осуществляются по синхронным механизмам. В неводных р-рителях к-ты и основания образуют преим. мол. комплексы. Каталитич. действие апротонных к-т обусловлено образованием из них и реагентов мол. реакционно-способных комплексов. Катиониты в Н-форме и нанесенные кислотные катализаторы обладают каталитич. активностью гл. обр. из-за наличия жидкой фазы, содержащей к-ту. Нанесенные кислотные катализаторы готовят нанесением на носитель (силикофосфат SiO
2.Р
2 О
5, силикагель, кварц, фосфаты) разл. жидких к-т, гл. обр. фосфорной. Каталитич. активность таких катализаторов зависит от кол-ва нанесенной к-ты на 1 г носителя и ее концентрации в жидкой фазе, зависящей от равновесного давления водяного пара над катализатором. Для характеристики ионизирующих св-в нанесенных кислотных катализаторов можно использовать такие же ф-ции а
Кaтf
P/f
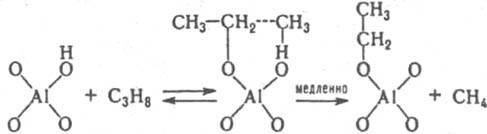
PKaт, как и для р-ров. Специфич. св-во практически всех гетерог. кислотно-основных катализаторов наличие на их пов-сти центров разл. силы (кислотной или основной), что обусловлено неоднородностью пов-сти твердых тел. Из-за наличия подобных центров образуются сильно поляризованные комплексы реагента с катализатором. Энергетически выгодными являются синхронно протекающие лимитирующие стадии. Так, крекинг парафинов на Аl
2 О
3 может протекать по схеме:
 Лит.
Лит. Гам мет Л , Основы физической органической химии, пер. с англ., М., 1972; Танабе К . Твердые кислоты и основания, пер. с англ., М., 1973, Белл Р , Протон в химии, пер. с англ., М., 1977; Виниик М И , "Кинетика и катализ", 1980. т 21. в. I.e. 136 58. Казанский В Б . там же. 1987. т 28. в. I, с. 47 60
МИ Винник  В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.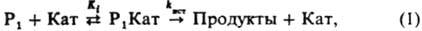 где Кат-разл. формы катализатора: недиссоциир. к-ты или основания, ионы или ионные пары, образующиеся при их ионизации; P1 Кат-комплексы; К i - константа равновесия образования комплексов Р 1 Кат; k ист - элементарная константа скорости превращ. комплексов в продукты. В случае р-ции двух реагентов (P1+Р 2: Продукты; Р 2+Р 2: Продукты) реакционноспособный комплекс образуется, как правило, из комплекса одного реагента с несвязанным в комплекс др. реагентом:
где Кат-разл. формы катализатора: недиссоциир. к-ты или основания, ионы или ионные пары, образующиеся при их ионизации; P1 Кат-комплексы; К i - константа равновесия образования комплексов Р 1 Кат; k ист - элементарная константа скорости превращ. комплексов в продукты. В случае р-ции двух реагентов (P1+Р 2: Продукты; Р 2+Р 2: Продукты) реакционноспособный комплекс образуется, как правило, из комплекса одного реагента с несвязанным в комплекс др. реагентом: 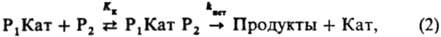 где К к -константа равновесия образования комплексов Р 1 Kат Р 2. Константы равновесия Ki и К к выражают ур-ниями:
где К к -константа равновесия образования комплексов Р 1 Kат Р 2. Константы равновесия Ki и К к выражают ур-ниями: 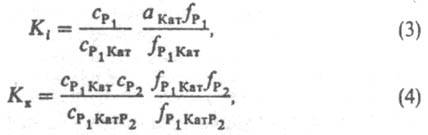 где (здесь и далее) а, с, f -соотв. термодинамич. активность, концентрация и коэф. активности реагирующих частиц; aKатfP1/fP1Кат - ф-ция, характеризующая способность среды переводить реагенты в комплексы РКат. При варьировании в широких пределах с Кат реализуются (особенно в р-рах) неск. маршрутов р-ции - хим. превращений, приводящих к образованию одних и тех же продуктов через реакционноспособные комплексы (РК) разл. состава. В р-ре с постоянной с Кат скорость р-ции по каждому маршруту Wi выражается ур-нием:
где (здесь и далее) а, с, f -соотв. термодинамич. активность, концентрация и коэф. активности реагирующих частиц; aKатfP1/fP1Кат - ф-ция, характеризующая способность среды переводить реагенты в комплексы РКат. При варьировании в широких пределах с Кат реализуются (особенно в р-рах) неск. маршрутов р-ции - хим. превращений, приводящих к образованию одних и тех же продуктов через реакционноспособные комплексы (РК) разл. состава. В р-ре с постоянной с Кат скорость р-ции по каждому маршруту Wi выражается ур-нием: 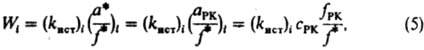 где (k ист)i - элементарная константа скорости по i-му маршруту, а* и f* - относятся к активир. комплексу. Из опытных данных следует, что множитель f РК/f* не изменяется при варьировании с Кат и его приравнивают к единице. В р-ре с постоянной с Кат наблюдаемая скорость р-ции
где (k ист)i - элементарная константа скорости по i-му маршруту, а* и f* - относятся к активир. комплексу. Из опытных данных следует, что множитель f РК/f* не изменяется при варьировании с Кат и его приравнивают к единице. В р-ре с постоянной с Кат наблюдаемая скорость р-ции 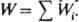 Экспериментально определяют эффективную константу скорости k эфф, характеризующую скорость р-ции при постоянной т-ре и наличии катализатора определенного состава. В ур-ниях для связи f эфф со св-вами катализатора учитывают все его комплексы с реагентом: реакционноспособные (РКат) РК и нереакционноспособные (РКат) НРК. Напр., при кислотном гидролизе амидов, анилидов ионизированная по атому азота форма является реакционноспособной, ионизированная по карбонильной группе - либо намного менее реакционноспособна, либо нереакционноспособна. Для описания влияния ионизирующих св-в среды на k эфф совместно решают ур-ние материального баланса для текущих концентраций реагентов и ур-ния (3) и (5) в случае р-ции одного реагента и дополнительно ур-ние (4) для р-ции двух реагентов. напр. для р-ции, протекающей по схеме (2):
Экспериментально определяют эффективную константу скорости k эфф, характеризующую скорость р-ции при постоянной т-ре и наличии катализатора определенного состава. В ур-ниях для связи f эфф со св-вами катализатора учитывают все его комплексы с реагентом: реакционноспособные (РКат) РК и нереакционноспособные (РКат) НРК. Напр., при кислотном гидролизе амидов, анилидов ионизированная по атому азота форма является реакционноспособной, ионизированная по карбонильной группе - либо намного менее реакционноспособна, либо нереакционноспособна. Для описания влияния ионизирующих св-в среды на k эфф совместно решают ур-ние материального баланса для текущих концентраций реагентов и ур-ния (3) и (5) в случае р-ции одного реагента и дополнительно ур-ние (4) для р-ции двух реагентов. напр. для р-ции, протекающей по схеме (2):  В случае р-ции двух реагентов, если один (Р 2) является компонентом р-рителя (напр., Н 2 О при гидролизе в водных р-рах), при условии с р2>>е р1 вычисляют эффективную константу скорости первого порядка, включающую термодинамич. активность р-рителя. В р-циях Р х с Р 2 в р-рах к-т и оснований реакционноспособный комплекс состава P1KaтP2 может получаться и в лимитирующей стадии из ионизир. формы одного реагента и неионизир. формы другого:
В случае р-ции двух реагентов, если один (Р 2) является компонентом р-рителя (напр., Н 2 О при гидролизе в водных р-рах), при условии с р2>>е р1 вычисляют эффективную константу скорости первого порядка, включающую термодинамич. активность р-рителя. В р-циях Р х с Р 2 в р-рах к-т и оснований реакционноспособный комплекс состава P1KaтP2 может получаться и в лимитирующей стадии из ионизир. формы одного реагента и неионизир. формы другого: 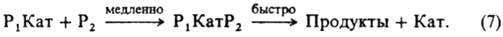 В этом случае для описания влияния ионизирующих св-в среды на k эфф пригодно ур-ние (6), при замене величины (fP2 с P2)/(К кfP1КатP2) на термодинамич. активность растворителя. Поскольку крайне редко удается установить прямыми физ. методами состав и концентрацию промежут. комплексов, в настоящее время основным методом установления их состава, детального механизма р-ции и вычисления величин К i и К к является кинетич. метод, основанный на применении ур-ний типа (6) для объяснения наблюдаемой зависимости k эфф от ионизирующей способности среды. Для этого измеряют k эфф в широком диапазоне с Кат в р-ре и подбирают ф-ции а Кат fP/fPКат для описания влияния среды на k эфф. наиб. исследованы каталитич. св-ва сильных к-т в водных р-рах. Ионизирующая способность таких р-ров обусловлена образованием комплексов реагента: 1) с сольватированным протоном и 2) с недиссоциированной к-той. К первым относятся протонир. форма реагента и ее комплексы с р-рителем. В этом случае а КатfP/fPKат выражают (для водных р-ров) ф-циями h0 =aH3O+fP/fPH+, h0aH2O и h0a2 Н2O, где h0 - измеренная индикаторным методом кислотность среды, f РН+ -коэф. активности протонир. формы реагента. Ко вторым относятся комплексы реагента с к-той (НА) и ее гидратами. При этом a Катf Р/f РКат кат принимает значения а НА, a НАa Н2O и др. При гидролизе нек-рых карбонильных соед. a КатfP/f РКат=cH5O2+ Однозначную информацию о составе реакционноспособных комплексов, как правило, получают на основании данных по изменению k эфф в р-рителе постоянного состава при варьировании с Кат в широких пределах в условиях малой степени связывания реагента в комплексы. наиб. простые зависимости получают для р-ции одного реагента, когда он равновесно связывается только в один реакционноспособный комплекс. В таком случае ур-ние (4) упрощается:
В этом случае для описания влияния ионизирующих св-в среды на k эфф пригодно ур-ние (6), при замене величины (fP2 с P2)/(К кfP1КатP2) на термодинамич. активность растворителя. Поскольку крайне редко удается установить прямыми физ. методами состав и концентрацию промежут. комплексов, в настоящее время основным методом установления их состава, детального механизма р-ции и вычисления величин К i и К к является кинетич. метод, основанный на применении ур-ний типа (6) для объяснения наблюдаемой зависимости k эфф от ионизирующей способности среды. Для этого измеряют k эфф в широком диапазоне с Кат в р-ре и подбирают ф-ции а Кат fP/fPКат для описания влияния среды на k эфф. наиб. исследованы каталитич. св-ва сильных к-т в водных р-рах. Ионизирующая способность таких р-ров обусловлена образованием комплексов реагента: 1) с сольватированным протоном и 2) с недиссоциированной к-той. К первым относятся протонир. форма реагента и ее комплексы с р-рителем. В этом случае а КатfP/fPKат выражают (для водных р-ров) ф-циями h0 =aH3O+fP/fPH+, h0aH2O и h0a2 Н2O, где h0 - измеренная индикаторным методом кислотность среды, f РН+ -коэф. активности протонир. формы реагента. Ко вторым относятся комплексы реагента с к-той (НА) и ее гидратами. При этом a Катf Р/f РКат кат принимает значения а НА, a НАa Н2O и др. При гидролизе нек-рых карбонильных соед. a КатfP/f РКат=cH5O2+ Однозначную информацию о составе реакционноспособных комплексов, как правило, получают на основании данных по изменению k эфф в р-рителе постоянного состава при варьировании с Кат в широких пределах в условиях малой степени связывания реагента в комплексы. наиб. простые зависимости получают для р-ции одного реагента, когда он равновесно связывается только в один реакционноспособный комплекс. В таком случае ур-ние (4) упрощается: 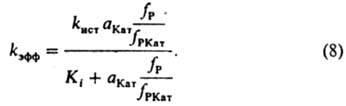 Опытным путем установлено, что в водных р-рах сильных к-т k ист не зависит от с Кат. К i, по определению, не должно зависеть от с Кат. Вопрос о влиянии состава смешанного р-рителя на k ист пока достаточно не исследован. В условиях, когда Ki и (a Катf Р)/f РКат соизмеримы, по ур-нию (8) вычисляют раздельно k ист и Ki. При а Катf Р/f РКат >> Ki<> величина k эфф=k ист; при k КатfP/f РКат<<Ki имеет место соотношение:
Опытным путем установлено, что в водных р-рах сильных к-т k ист не зависит от с Кат. К i, по определению, не должно зависеть от с Кат. Вопрос о влиянии состава смешанного р-рителя на k ист пока достаточно не исследован. В условиях, когда Ki и (a Катf Р)/f РКат соизмеримы, по ур-нию (8) вычисляют раздельно k ист и Ki. При а Катf Р/f РКат >> Ki<> величина k эфф=k ист; при k КатfP/f РКат<<Ki имеет место соотношение: 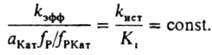 Ниже приведен пример, раскрывающий природу каталитич. действия водных р-ров к-т в условиях, когда реакционноспособный комплекс образуется и превращ. в продукты согласно схеме (1) при условии, что а КатfP/f РКат<<Ki. Ионизирующая способность среды из-за превращ. реагента в протонир. форму и ее комплексы с Н 2 О проявляется при наличии зависимостей К эфф/h0=const, k эфф(h0aH2О)=const k эфф/(h0a2H2O)=const. Если в р-ции k эфф/h0=const (lgk эфф+H0=const, где H0=-lgh0 - ф-ция кислотности Гаммета), то a катfP/f Кат=h0 и реакционноспособным комплексом является протонир. форма реагента РН 3 О +. Такая закономерность имеет место при проведении пинаколиновой перегруппировки в конц. H2SO4:
Ниже приведен пример, раскрывающий природу каталитич. действия водных р-ров к-т в условиях, когда реакционноспособный комплекс образуется и превращ. в продукты согласно схеме (1) при условии, что а КатfP/f РКат<<Ki. Ионизирующая способность среды из-за превращ. реагента в протонир. форму и ее комплексы с Н 2 О проявляется при наличии зависимостей К эфф/h0=const, k эфф(h0aH2О)=const k эфф/(h0a2H2O)=const. Если в р-ции k эфф/h0=const (lgk эфф+H0=const, где H0=-lgh0 - ф-ция кислотности Гаммета), то a катfP/f Кат=h0 и реакционноспособным комплексом является протонир. форма реагента РН 3 О +. Такая закономерность имеет место при проведении пинаколиновой перегруппировки в конц. H2SO4:  При варьировании с Kaт значение k эфф/(h0 а H2O) постоянно в р-циях дегидратации, напр. 2-фенил-2-пропанола в серной к-те, 2-метил-2-бутанола в азотной к-те. Следовательно, а KатfP/fPKaт равно h0 а H2O и реакционноспособным является комплекс молекулы воды с протонир. формой реагента. Имеется и пример постоянства k эфф/(h0a2H2O), что наблюдается в р-ции изотопного обмена атома кислорода в СН 3 ОН, протекающего в серной и хлорной к-тах. В этом случае а Kaт/fP/f РКaт=h0a2H2O и реакционноспособным является симметричный комплекс:
При варьировании с Kaт значение k эфф/(h0 а H2O) постоянно в р-циях дегидратации, напр. 2-фенил-2-пропанола в серной к-те, 2-метил-2-бутанола в азотной к-те. Следовательно, а KатfP/fPKaт равно h0 а H2O и реакционноспособным является комплекс молекулы воды с протонир. формой реагента. Имеется и пример постоянства k эфф/(h0a2H2O), что наблюдается в р-ции изотопного обмена атома кислорода в СН 3 ОН, протекающего в серной и хлорной к-тах. В этом случае а Kaт/fP/f РКaт=h0a2H2O и реакционноспособным является симметричный комплекс:  Ф-ции h0, h0 а H2O и h0 а 2H2O стандартизованы к воде, и в сильно разбавленных р-рах сильных к-т они численно равны концентрации ионов Н 5 О +2 в моль/л. В таких р-рах для приведенных выше р-ций при варьировании с Kaт должно соблюдаться постоянство значений k эфф/cH2O+. При гидролизе нек-рых амидов, анилидов, сложных эфиров k эфф/cH2O+ постоянно не только в разбавленных, но и в конц. водный р-рах НСlO4, H2SO4. Если гидролиз протекает по схеме (1), то реакционноспособный комплекс образуется из реагента и иона Н 5 О 2+, а выраженная в концентрациях константа равновесия KH5O2+; не изменяется при варьировании с Кат:
Ф-ции h0, h0 а H2O и h0 а 2H2O стандартизованы к воде, и в сильно разбавленных р-рах сильных к-т они численно равны концентрации ионов Н 5 О +2 в моль/л. В таких р-рах для приведенных выше р-ций при варьировании с Kaт должно соблюдаться постоянство значений k эфф/cH2O+. При гидролизе нек-рых амидов, анилидов, сложных эфиров k эфф/cH2O+ постоянно не только в разбавленных, но и в конц. водный р-рах НСlO4, H2SO4. Если гидролиз протекает по схеме (1), то реакционноспособный комплекс образуется из реагента и иона Н 5 О 2+, а выраженная в концентрациях константа равновесия KH5O2+; не изменяется при варьировании с Кат: 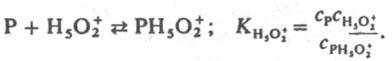 Не исключено, что k эфф/cH2O+=const из-за того, что р-ция протекает по схеме (7) Ионизирующая способность среды из-за комплексообразования реагента с молекулами недиссоциир. сильной к-ты и ее гидратом проявляется при наличии зависимостей k эфф/aHA=const, k эфф/(aHAaH2O)=const и др. В первом случае aKaт=const и реакци онноспособный комплекс имеет состав РИА; такая закономерность, напр., реализуется при дегидратации b-фенил-b-гидроксипропионовой к-ты и 2-(4-мето-ксифенил)-2-пропанола в серной к-те. Во втором случае а катfP/fPKат=а HА а H2O и комплекс имеет состав РНАН 2 О. Гидрат НА. Н 2 О можно рассматривать и как ионную пару Н 3 О + А -. Каталитич. активность гидратов сильных к-т проявляется в р-циях дегидратации 1-фенилэтанола в хлорной к-те, гидратации цис -коричной к-ты и рацемизации b-фенил-b-гидроксипропионовой к-ты в серной к-те. Согласно ур-нию (6), должен наблюдаться максимум k эфф в зависимости от с Кат, если наряду с реакционноспособными образуются и нереакционноспособные комплексы и при увеличении с Кат значение a Кат/fP/fPKат для нeрeакционноспособных комплексов возрастает быстрее и более резко, чем для реакционноспособных. Напр., если a КатfP/fPKaт равно с H5O2+ для реакционноспособных комплексов и равно h0, либо h0aH2O для нереакционноспособных. В водных р-рах слабых к-т каталитич. активность проявляют ионы и недиссоциир. молекулы к-ты. Взаимосвязь между каталитич. активностью слабых к-т и их константами диссоциации в нек-рых случаях удается описать корреляц. ур-нием Брёнстеда. В сильно разбавленных водных р-рах оснований ндблюдается постоянство k эфф/cOH -при варьировании с OH-. Обоснованных количеств. характеристик ионизирующей способности умеренно конц. и конц. р-ров оснований пока нет. Добавление солей к водным р-рам к-т и оснований существенно изменяет их каталитич. активность; в случае слабых к-т и оснований изменяется степень их диссоциации на ионы из-за наличия общего иона и увеличения ионной силы р-ра. В случае сильных к-т изменяются величины h0, а НА, а Н2O, что приводит к увеличению относит, концентрации комплексов, образующихся из частиц Н 3 О + А -, НА, а также усилению реакц. способности ионов Н 5 О 2+, напр. при гидролизе в условиях, когда a КатfP/fPKат=с H2O+. В случае сильных оснований катионы металлов усиливают каталитич. действие сольватир. ионов ОН -. Лимитирующие стадии катализируемых к-тами и основаниями р-ций часто осуществляются по синхронным механизмам. В неводных р-рителях к-ты и основания образуют преим. мол. комплексы. Каталитич. действие апротонных к-т обусловлено образованием из них и реагентов мол. реакционно-способных комплексов. Катиониты в Н-форме и нанесенные кислотные катализаторы обладают каталитич. активностью гл. обр. из-за наличия жидкой фазы, содержащей к-ту. Нанесенные кислотные катализаторы готовят нанесением на носитель (силикофосфат SiO2.Р 2 О 5, силикагель, кварц, фосфаты) разл. жидких к-т, гл. обр. фосфорной. Каталитич. активность таких катализаторов зависит от кол-ва нанесенной к-ты на 1 г носителя и ее концентрации в жидкой фазе, зависящей от равновесного давления водяного пара над катализатором. Для характеристики ионизирующих св-в нанесенных кислотных катализаторов можно использовать такие же ф-ции а КaтfP/fPKaт, как и для р-ров. Специфич. св-во практически всех гетерог. кислотно-основных катализаторов наличие на их пов-сти центров разл. силы (кислотной или основной), что обусловлено неоднородностью пов-сти твердых тел. Из-за наличия подобных центров образуются сильно поляризованные комплексы реагента с катализатором. Энергетически выгодными являются синхронно протекающие лимитирующие стадии. Так, крекинг парафинов на Аl2 О 3 может протекать по схеме:
Не исключено, что k эфф/cH2O+=const из-за того, что р-ция протекает по схеме (7) Ионизирующая способность среды из-за комплексообразования реагента с молекулами недиссоциир. сильной к-ты и ее гидратом проявляется при наличии зависимостей k эфф/aHA=const, k эфф/(aHAaH2O)=const и др. В первом случае aKaт=const и реакци онноспособный комплекс имеет состав РИА; такая закономерность, напр., реализуется при дегидратации b-фенил-b-гидроксипропионовой к-ты и 2-(4-мето-ксифенил)-2-пропанола в серной к-те. Во втором случае а катfP/fPKат=а HА а H2O и комплекс имеет состав РНАН 2 О. Гидрат НА. Н 2 О можно рассматривать и как ионную пару Н 3 О + А -. Каталитич. активность гидратов сильных к-т проявляется в р-циях дегидратации 1-фенилэтанола в хлорной к-те, гидратации цис -коричной к-ты и рацемизации b-фенил-b-гидроксипропионовой к-ты в серной к-те. Согласно ур-нию (6), должен наблюдаться максимум k эфф в зависимости от с Кат, если наряду с реакционноспособными образуются и нереакционноспособные комплексы и при увеличении с Кат значение a Кат/fP/fPKат для нeрeакционноспособных комплексов возрастает быстрее и более резко, чем для реакционноспособных. Напр., если a КатfP/fPKaт равно с H5O2+ для реакционноспособных комплексов и равно h0, либо h0aH2O для нереакционноспособных. В водных р-рах слабых к-т каталитич. активность проявляют ионы и недиссоциир. молекулы к-ты. Взаимосвязь между каталитич. активностью слабых к-т и их константами диссоциации в нек-рых случаях удается описать корреляц. ур-нием Брёнстеда. В сильно разбавленных водных р-рах оснований ндблюдается постоянство k эфф/cOH -при варьировании с OH-. Обоснованных количеств. характеристик ионизирующей способности умеренно конц. и конц. р-ров оснований пока нет. Добавление солей к водным р-рам к-т и оснований существенно изменяет их каталитич. активность; в случае слабых к-т и оснований изменяется степень их диссоциации на ионы из-за наличия общего иона и увеличения ионной силы р-ра. В случае сильных к-т изменяются величины h0, а НА, а Н2O, что приводит к увеличению относит, концентрации комплексов, образующихся из частиц Н 3 О + А -, НА, а также усилению реакц. способности ионов Н 5 О 2+, напр. при гидролизе в условиях, когда a КатfP/fPKат=с H2O+. В случае сильных оснований катионы металлов усиливают каталитич. действие сольватир. ионов ОН -. Лимитирующие стадии катализируемых к-тами и основаниями р-ций часто осуществляются по синхронным механизмам. В неводных р-рителях к-ты и основания образуют преим. мол. комплексы. Каталитич. действие апротонных к-т обусловлено образованием из них и реагентов мол. реакционно-способных комплексов. Катиониты в Н-форме и нанесенные кислотные катализаторы обладают каталитич. активностью гл. обр. из-за наличия жидкой фазы, содержащей к-ту. Нанесенные кислотные катализаторы готовят нанесением на носитель (силикофосфат SiO2.Р 2 О 5, силикагель, кварц, фосфаты) разл. жидких к-т, гл. обр. фосфорной. Каталитич. активность таких катализаторов зависит от кол-ва нанесенной к-ты на 1 г носителя и ее концентрации в жидкой фазе, зависящей от равновесного давления водяного пара над катализатором. Для характеристики ионизирующих св-в нанесенных кислотных катализаторов можно использовать такие же ф-ции а КaтfP/fPKaт, как и для р-ров. Специфич. св-во практически всех гетерог. кислотно-основных катализаторов наличие на их пов-сти центров разл. силы (кислотной или основной), что обусловлено неоднородностью пов-сти твердых тел. Из-за наличия подобных центров образуются сильно поляризованные комплексы реагента с катализатором. Энергетически выгодными являются синхронно протекающие лимитирующие стадии. Так, крекинг парафинов на Аl2 О 3 может протекать по схеме:  Лит. Гам мет Л , Основы физической органической химии, пер. с англ., М., 1972; Танабе К . Твердые кислоты и основания, пер. с англ., М., 1973, Белл Р , Протон в химии, пер. с англ., М., 1977; Виниик М И , "Кинетика и катализ", 1980. т 21. в. I.e. 136 58. Казанский В Б . там же. 1987. т 28. в. I, с. 47 60 МИ Винник
Лит. Гам мет Л , Основы физической органической химии, пер. с англ., М., 1972; Танабе К . Твердые кислоты и основания, пер. с англ., М., 1973, Белл Р , Протон в химии, пер. с англ., М., 1977; Виниик М И , "Кинетика и катализ", 1980. т 21. в. I.e. 136 58. Казанский В Б . там же. 1987. т 28. в. I, с. 47 60 МИ Винник