: в бесконечно разбавленном р-ре электролита перенос электричества осуществляется всеми ионами независимо друг от друга. Вследствие этого общая молярная электрич. проводимость такого р-ра L° равна сумме электрич. проводимостей l°
i отдельных ионов, а разность молярных электрич. проводимостей двух р-ров солей с общим катионом не зависит от природы этого катиона, напр.
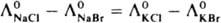
. При увеличении концентрации р-ра вследствие взаимод. ионов их движение уже не является независимым и К. з. не выполняется. Практич. использование К. з. состоит в нахождении L° р-ров слабых электролитов. Для этого привлекают данные о проводимости разб. р-ров сильных электролитов, к-рые полностью диссоциируют на те же ионы, что и изучаемый слабый электролит. Напр., для нахождения L°
СH3COOH параллельно измеряют молярные электрич. проводимости р-ров НС1 и CH
3COONa и числа переноса t
i ионов Н
+ и СН
3 СОО
- при разл. концентрациях с; полученные зависимости
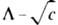
и
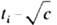
экстраполируют к
с=0. Согласно К. з.,
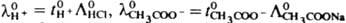
и
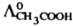
=
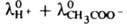
. Независимость l°
- при заданной т-ре от природы катиона соли служит эксперим. подтверждением К. з. Закон установлен экспериментально Ф. Кольраушем в 1879.
Лит.: Робинсон Р. А., Стоке Р. Г., Растворы электролитов, пер. с англ., М., 1963; Дамаск и н Б. Б., Петрий О. А., Основы теоретической электрохимии, М., 1978.
Б. Б. Дамаскин.
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.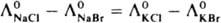 . При увеличении концентрации р-ра вследствие взаимод. ионов их движение уже не является независимым и К. з. не выполняется. Практич. использование К. з. состоит в нахождении L° р-ров слабых электролитов. Для этого привлекают данные о проводимости разб. р-ров сильных электролитов, к-рые полностью диссоциируют на те же ионы, что и изучаемый слабый электролит. Напр., для нахождения L° СH3COOH параллельно измеряют молярные электрич. проводимости р-ров НС1 и CH3COONa и числа переноса ti ионов Н + и СН 3 СОО - при разл. концентрациях с; полученные зависимости
. При увеличении концентрации р-ра вследствие взаимод. ионов их движение уже не является независимым и К. з. не выполняется. Практич. использование К. з. состоит в нахождении L° р-ров слабых электролитов. Для этого привлекают данные о проводимости разб. р-ров сильных электролитов, к-рые полностью диссоциируют на те же ионы, что и изучаемый слабый электролит. Напр., для нахождения L° СH3COOH параллельно измеряют молярные электрич. проводимости р-ров НС1 и CH3COONa и числа переноса ti ионов Н + и СН 3 СОО - при разл. концентрациях с; полученные зависимости 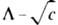 и
и 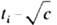 экстраполируют к с=0. Согласно К. з.,
экстраполируют к с=0. Согласно К. з., 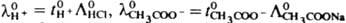 и
и 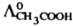 =
= 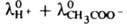 . Независимость l°- при заданной т-ре от природы катиона соли служит эксперим. подтверждением К. з. Закон установлен экспериментально Ф. Кольраушем в 1879. Лит.: Робинсон Р. А., Стоке Р. Г., Растворы электролитов, пер. с англ., М., 1963; Дамаск и н Б. Б., Петрий О. А., Основы теоретической электрохимии, М., 1978. Б. Б. Дамаскин.
. Независимость l°- при заданной т-ре от природы катиона соли служит эксперим. подтверждением К. з. Закон установлен экспериментально Ф. Кольраушем в 1879. Лит.: Робинсон Р. А., Стоке Р. Г., Растворы электролитов, пер. с англ., М., 1963; Дамаск и н Б. Б., Петрий О. А., Основы теоретической электрохимии, М., 1978. Б. Б. Дамаскин.