(от лат. constans, род. падеж constantis - постоянный, неизменный), величина, определяющая для данной хим. р-ции соотношение между термодинамич. активностями исходных в-в и продуктов в состоянии хим. равновесия. В общем случае р-ции
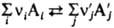
где v
i и
v'j - стехиометрич. числа исходных в-в А
i (i=1,2,..., q)
и продуктов р-ции А
'j (j=1, 2, ..., r), активности к-рых соотв.
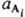
и
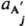
, константа равновесия
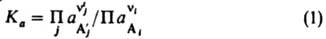
(П - оператор произведения). Это выражение является мат. записью
действующих масс закона;
оно справедливо для всех состояний хим. равновесия системы независимо от ее начального состава и наличия в ней др. хим. р-ций. К. р. связана со стандартным изменением энергии Гиббса DG° рассматриваемой р-ции при данных т-ре Т
и давлении рсоотношением: RTln
<>a=->DG° (R-газовая постоянная). Зависимости
К а от т-ры и давления выражаются соотношениями:
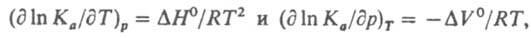
где DH° и DV° - соотв. стандартные изменения энтальпии и объема системы при данной р-ции. Численное значение
К а зависит от способа выбора
стандартного состояния для каждого из участвующих в р-ции в-в. Для р-ций в р-рах в качестве стандартного состояния реагентов м. б. приняты чистые жидкости при тех же Ти
р; тогда
К а не зависит от природы р-рителя; последний в этом случае определяет значения коэф. активности, связывающих активности в-в с их концентрацией. Для разб. р-ров часто в качестве стандартных состояний реагентов принимают их гипотетич. состояния в предельно разб. р-ре в том же р-рителе, но при единичной концентрации (для рассматриваемой концентрац. шкалы); тогда активность реагента при предельном разбавлении совпадает с его концентрацией, а значение
К а зависит от природы р-рителя. Изменение
К а при перемене р-рителя отражает изменение
сольватации - взаимод. молекул реагирующих в-в с молекулами р-рителя. Если в р-ции принимают участие твердые или жидкие в-ва, составляющие индивидуальную фазу, их состояния принято считать стандартными, поэтому их активности равны единице и не входят в выражение для
К а (хотя соответствующие вклады в изменение энергии Гиббса учитываются). Для р-ций в газах в выражение для К. р. вместо активностей авходят
летучести f реагирующих в-в; К. р. в этом случае обозначается
<>f.
Если реагирующую систему можно считать смесью идеальных газов, летучесть любого из компонентов смеси равна его парциальному давлению p
i, что позволяет выражать К. р. через p
i (обозначается
К р и численно совпадает с
<>f)
или молярные концентрации с
i=p
i/RT (обозначается
<>f).
Эти две К. р. связаны соотношением: К
c<>p/(RT)
Dv, где
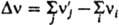
- изменение числа молей газообразных в-в в результате р-ции. Зависимость
<>p (и К
с) от т-ры выражается ур-нием Вант-Гоффа dlnK
p/dT=DH°/RT
2, к-рое наз. также уравнением изобары реакции, поскольку содержит в правой части изобарный тепловой эффект р-ции DH°. Аналогичное ур-ние dlnK
c/dT=DU°/RT
2 содержит изохорный тепловой эффект р-ции DU°=DH°-RТDv и потому известно как уравнение изохоры реакции. Расчет К. р. выполняется с применением таблиц термодинамич. св-в в-в по ур-нию: RTlnК
р=TDS
0-DH°, где DS° - стандартное изменение энтропии системы при р-ции; возможен также расчет
К р методами статистич. термодинамики, в осн. для р-ций без участия конденсир. фаз. В случае р-ций в р-рах для расчета
К а используют
корреляционные соотношения. Определение К. р. всех протекающих в системе р-ций и решение ур-ний (1) совместно с ур-ниями материального баланса позволяет отыскать равновесные составы системы при заданных начальных условиях.
Лит.: Киреев В. А., Методы практических расчетов в термодинамике химических реакций, 2 изд., М., 1975; Жоров Ю. М., Термодинамика химических процессов, М., 1985. См. также лит. при ст.
Химическая термодинамика. В. А. Михайлов.  В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.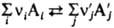 где vi и v'j - стехиометрич. числа исходных в-в А i (i=1,2,..., q) и продуктов р-ции А 'j (j=1, 2, ..., r), активности к-рых соотв.
где vi и v'j - стехиометрич. числа исходных в-в А i (i=1,2,..., q) и продуктов р-ции А 'j (j=1, 2, ..., r), активности к-рых соотв. 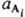 и
и 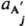 , константа равновесия
, константа равновесия 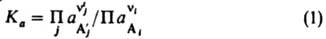 (П - оператор произведения). Это выражение является мат. записью действующих масс закона; оно справедливо для всех состояний хим. равновесия системы независимо от ее начального состава и наличия в ней др. хим. р-ций. К. р. связана со стандартным изменением энергии Гиббса DG° рассматриваемой р-ции при данных т-ре Т и давлении рсоотношением: RTln<>a=->DG° (R-газовая постоянная). Зависимости К а от т-ры и давления выражаются соотношениями:
(П - оператор произведения). Это выражение является мат. записью действующих масс закона; оно справедливо для всех состояний хим. равновесия системы независимо от ее начального состава и наличия в ней др. хим. р-ций. К. р. связана со стандартным изменением энергии Гиббса DG° рассматриваемой р-ции при данных т-ре Т и давлении рсоотношением: RTln<>a=->DG° (R-газовая постоянная). Зависимости К а от т-ры и давления выражаются соотношениями: 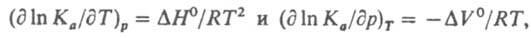 где DH° и DV° - соотв. стандартные изменения энтальпии и объема системы при данной р-ции. Численное значение К а зависит от способа выбора стандартного состояния для каждого из участвующих в р-ции в-в. Для р-ций в р-рах в качестве стандартного состояния реагентов м. б. приняты чистые жидкости при тех же Ти р; тогда К а не зависит от природы р-рителя; последний в этом случае определяет значения коэф. активности, связывающих активности в-в с их концентрацией. Для разб. р-ров часто в качестве стандартных состояний реагентов принимают их гипотетич. состояния в предельно разб. р-ре в том же р-рителе, но при единичной концентрации (для рассматриваемой концентрац. шкалы); тогда активность реагента при предельном разбавлении совпадает с его концентрацией, а значение К а зависит от природы р-рителя. Изменение К а при перемене р-рителя отражает изменение сольватации - взаимод. молекул реагирующих в-в с молекулами р-рителя. Если в р-ции принимают участие твердые или жидкие в-ва, составляющие индивидуальную фазу, их состояния принято считать стандартными, поэтому их активности равны единице и не входят в выражение для К а (хотя соответствующие вклады в изменение энергии Гиббса учитываются). Для р-ций в газах в выражение для К. р. вместо активностей авходят летучести f реагирующих в-в; К. р. в этом случае обозначается <>f. Если реагирующую систему можно считать смесью идеальных газов, летучесть любого из компонентов смеси равна его парциальному давлению pi, что позволяет выражать К. р. через pi (обозначается К р и численно совпадает с <>f) или молярные концентрации с i=pi/RT (обозначается <>f). Эти две К. р. связаны соотношением: К c<>p/(RT)Dv, где
где DH° и DV° - соотв. стандартные изменения энтальпии и объема системы при данной р-ции. Численное значение К а зависит от способа выбора стандартного состояния для каждого из участвующих в р-ции в-в. Для р-ций в р-рах в качестве стандартного состояния реагентов м. б. приняты чистые жидкости при тех же Ти р; тогда К а не зависит от природы р-рителя; последний в этом случае определяет значения коэф. активности, связывающих активности в-в с их концентрацией. Для разб. р-ров часто в качестве стандартных состояний реагентов принимают их гипотетич. состояния в предельно разб. р-ре в том же р-рителе, но при единичной концентрации (для рассматриваемой концентрац. шкалы); тогда активность реагента при предельном разбавлении совпадает с его концентрацией, а значение К а зависит от природы р-рителя. Изменение К а при перемене р-рителя отражает изменение сольватации - взаимод. молекул реагирующих в-в с молекулами р-рителя. Если в р-ции принимают участие твердые или жидкие в-ва, составляющие индивидуальную фазу, их состояния принято считать стандартными, поэтому их активности равны единице и не входят в выражение для К а (хотя соответствующие вклады в изменение энергии Гиббса учитываются). Для р-ций в газах в выражение для К. р. вместо активностей авходят летучести f реагирующих в-в; К. р. в этом случае обозначается <>f. Если реагирующую систему можно считать смесью идеальных газов, летучесть любого из компонентов смеси равна его парциальному давлению pi, что позволяет выражать К. р. через pi (обозначается К р и численно совпадает с <>f) или молярные концентрации с i=pi/RT (обозначается <>f). Эти две К. р. связаны соотношением: К c<>p/(RT)Dv, где 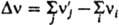 - изменение числа молей газообразных в-в в результате р-ции. Зависимость <>p (и К с) от т-ры выражается ур-нием Вант-Гоффа dlnKp/dT=DH°/RT2, к-рое наз. также уравнением изобары реакции, поскольку содержит в правой части изобарный тепловой эффект р-ции DH°. Аналогичное ур-ние dlnKc/dT=DU°/RT2 содержит изохорный тепловой эффект р-ции DU°=DH°-RТDv и потому известно как уравнение изохоры реакции. Расчет К. р. выполняется с применением таблиц термодинамич. св-в в-в по ур-нию: RTlnК р=TDS0-DH°, где DS° - стандартное изменение энтропии системы при р-ции; возможен также расчет К р методами статистич. термодинамики, в осн. для р-ций без участия конденсир. фаз. В случае р-ций в р-рах для расчета К а используют корреляционные соотношения. Определение К. р. всех протекающих в системе р-ций и решение ур-ний (1) совместно с ур-ниями материального баланса позволяет отыскать равновесные составы системы при заданных начальных условиях. Лит.: Киреев В. А., Методы практических расчетов в термодинамике химических реакций, 2 изд., М., 1975; Жоров Ю. М., Термодинамика химических процессов, М., 1985. См. также лит. при ст. Химическая термодинамика. В. А. Михайлов.
- изменение числа молей газообразных в-в в результате р-ции. Зависимость <>p (и К с) от т-ры выражается ур-нием Вант-Гоффа dlnKp/dT=DH°/RT2, к-рое наз. также уравнением изобары реакции, поскольку содержит в правой части изобарный тепловой эффект р-ции DH°. Аналогичное ур-ние dlnKc/dT=DU°/RT2 содержит изохорный тепловой эффект р-ции DU°=DH°-RТDv и потому известно как уравнение изохоры реакции. Расчет К. р. выполняется с применением таблиц термодинамич. св-в в-в по ур-нию: RTlnК р=TDS0-DH°, где DS° - стандартное изменение энтропии системы при р-ции; возможен также расчет К р методами статистич. термодинамики, в осн. для р-ций без участия конденсир. фаз. В случае р-ций в р-рах для расчета К а используют корреляционные соотношения. Определение К. р. всех протекающих в системе р-ций и решение ур-ний (1) совместно с ур-ниями материального баланса позволяет отыскать равновесные составы системы при заданных начальных условиях. Лит.: Киреев В. А., Методы практических расчетов в термодинамике химических реакций, 2 изд., М., 1975; Жоров Ю. М., Термодинамика химических процессов, М., 1985. См. также лит. при ст. Химическая термодинамика. В. А. Михайлов.